Technika Grzewcza i Sanitarna
INSTAL-MNOCHY
ul. Parkowa 1 b
47-100 Błotnica Strzelecka
Tel.: +48 77 4619065
Fax: +48 77 4619065
E-mail: biuro@instal-mnochy.pl
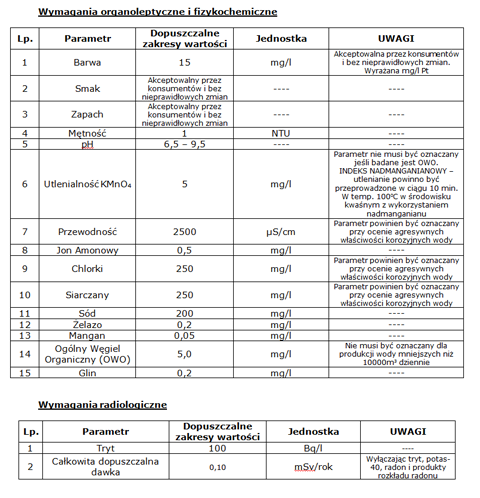
Stacje zmiękczania i uzdatniania wody - zagadnienia teoretyczne
Od prawidłowej oceny składu chemicznego wody zależy dobór odpowiedniej metody uzdatniania wody oraz efektywność usuwania z niej zanieczyszczeń.
Obecnie w Polsce wymagania dotyczące jakości wody przeznaczonej do spożycia przez ludzi reguluje Rozporządzenie Ministra Zdrowia z dnia 29.03.2007r. (Dz. U. nr 61 , poz. 417 ze zm. Dz.U.nr 72, poz. 72, poz. 466)
W codziennym wykorzystywaniu wody na cele bytowo-gospodarcze najczęściej zgłaszanymi problemami jakości wody są: mętność, barwa, twardość ogólna, żelazo, mangan i chlor. Zazwyczaj są to problemy związane z właściwościami organoleptycznymi wody. Twarda woda powoduje osadzanie się kamienia na urządzeniach gospodarstwa domowego, żelazo i mangan powodują wyraźne brunatne zacieki na armaturze sanitarnej a chlor nadaje wodzie nieprzyjemny często „odpychający” zapach. Niemniej należy zaznaczyć że woda wodociągowa płynąca w „przysłowiowym kranie” jest wodą zdatną do picia gdyż musi spełniać wymogi w/w rozporządzenia.
Dużym problemem są składniki często obecne w wodzie których nadmiaru nie jesteśmy w stanie rozpoznać organoleptycznie. Niejednokrotnie właściciele przydomowych studni nie zdają sobie sprawy, ze pijąc wodę pozornie „czystą” dostarczają do organizmu np. azotanów czy siarczanów w ilościach znacznie przekraczających wymogi Ministra Zdrowia. Skutki kumulacji tych substancji w organizmie człowieka mogą być dramatyczne dla zdrowia ludzi.
Najbardziej schematyczny podział metod uzdatniania wody w zależności od rodzaju wskaźnika, którego nadmiar jest uciążliwy i wymaga redukcji przedstawia się następująco:
- MĘTNOŚĆ, BARWA, ZAPACH, CHLOR – filtracja na węglu aktywnym
- ŻELAZO OGÓLNE – odżelazianie
- MANGAN – odmanganianie
- TWARDOŚĆ OGÓLNA – zmiękczanie / odwrócona osmoza
- AZOTANY i SIARCZANY – wymiana jonowa / odwrócona osmoza
Oczywiście wskaźników jakości wody jest znacznie więcej podobnie jak metod uzdatniania wody jednak w tym pragniemy przedstawić Państwu jedynie ogólny zarys problematyki związanej z uzdatnianiem wody.
Krótka charakterystyka wybranych wskaźników jakości wody.
MĘTNOŚĆ – wywoływana jest głównie przez rozproszone cząsteczki koloidalne i zawiesiny w szczególności cząsteczki pylasto-ilaste, wodorotlenki żelaza, węglany, nierozpuszczalne związki organiczne, mikroorganizmy i inne. Wody podziemne charakteryzują się na ogół wysoką przezroczystością a więc małą mętnością co jest w przeważającej mierze zasługą procesów filtracji zachodzących w ośrodku hydrogeologicznym. W wielu przypadkach mętność w eksploatowanych wodach podziemnych Pojawia się dopiero po wydobyciu tych wód na powierzchnię i kontakcie z powietrzem atmosferycznym. W klasycznym przypadku występuje wytrącanie wodorotlenków żelaza oraz węglanów co z kolei ma swoje odzwierciedlenie we wzroście mętności. Badanie mętności powinno być wykonywane w terenie bezpośrednio u źródła wody.
Mętność można wyrażać w skali krzemionkowej, gdzie za jednostkę mętności przyjmuje się wodę zawierającą 1 mg/dm3 SiO3 o średnicy cząstek ok. 100µm. jest to system jednostek określany jako JTU. W powszechniejszym użyciu z uwag na większą dokłądość jest tzw. pomiar turbidymetryczny lub nefelometryczny. Istota pomiaru turbindymetrycznego polega na pomiarze absorpcji światła przechodzącego przez warstwę wody o określonej grubości. Pomiar nefelometryczny odzwierciedla intensywność światła rozproszonego od cząstek, które powodują mętność. Mętność podawana jest wówczas w jednostkach NTU.
BARWA – przy wykorzystaniu wody do celów pitnych obserwujemy, że jest ona bezbarwna. Głównymi sprawcami zabarwienia wód podziemnych eksploatowanych na cele bytowo-gospodarcze jest obecność zawiesiny, substancji koloidalnych i rozpuszczonych. Rozróżniamy barwę tzw. pozorna wywołaną przez zawiesimy zawarte w ujmowanej wodzie oraz barwę rzeczywistą wywołana rozpuszczonymi związkami w wodzie. Najczęstszą przyczyną zabarwienia ujmowanych wód podziemnych jest obecność substancji organicznych. Takie wody wykazują zabarwienie żółte, pomarańczowe, brunatne, rdzawe, wiśniowe, aż do koloru praktycznie czarnego. Należy zaznaczyć, ze barwa wody może być również wywołana czynnikami antropogenicznymi. Intensywność zabarwienia wody podaje się w skali Hazena. Barwę wody określa się przez porównanie ze skalą wzorców platynowych i podaje w mg Pt/dm3.
SMAK i POSMAK – jest to cecha wody wywołana przez substancje w niej rozpuszczone, bądź zawiesiny. W przypadku oznaczania tych wskaźników bardzo ważne znaczenia ma temperatura wody. Dodatkowym przy oznaczaniu smaku duże znaczenie mają indywidualna wrażliwość smakowa osoby wykonującej badanie. Rozróżnia się 4 podstawowe rodzaje smaku: słony, gorzki, słodki i kwaśny. Wszystkie pozostałe odczucia smakowe określane są mianem posmaku np., posmak metaliczny, fenolowy lub mdły. Do określania smaku stosuje się 6 stopniową skalę:
- 0 – brak smaku
- 1 – smak bardzo słaby
- 2 – smak słaby
- 3 – smak wyraźny
- 4 – smak silny
- 5 – smak bardzo silny
ZAPACH – obok smaku to podstawowa cecha organoleptyczna przy ocenie przydatności wody do konsumpcji wody. Zgodnie z obowiązującymi przepisami zapach wody musi być akceptowalny przez konsumentów i bez nieprawidłowych zmian. Generalnie wody podziemne nie wykazują zapachu. Wyjątek mogą stanowić te wody które miały bezpośredni kontakt z bagnami torfowiskami, zanieczyszczeniami antropogenicznymi, lub wody złożowe i mineralne. Przy określaniu zapachu wody podobnie jak w przypadku smaku i posmaku duże znaczenie odgrywa temperatura wody, odczucia węchowe badającego oraz ilość i rodzaj substancji rozpuszczonych lub zawieszonych w wodzie. Rozróżnia się 3 rodzaje zapachu:
- R- roślinne – np. torfowy, trawiasty, kwiatowy, ziemisty, itp.
- G – gnilne – np. stęchły zbutwiały, siarkowodoru, pleśni, itp.
- S – specyficzne – np. benzyny, alkoholu, smoły, fekalny, itp.
Zapachy R i G, to zapachy pochodzenia naturalnego, natomiast zapachy S wskazują zwykle na zanieczyszczenia antropogeniczne związkami organicznymi bądź nieorganicznymi.
Intensywność zapachu określa się za pocą 6 stopniowej skali:
- 0 – brak zapachu
- 1 – zapach bardzo słaby
- 2 – zapach słaby
- 3 – zapach wyraźny
- 4 – zapach silny
- 5 – zapach bardzo silny
ODCZYN (pH) – określamy jako ujemny logarytm ze stężenia jonów wodorowych. pH = -lg[H+]. Jednostek logarytmicznych używa się dlatego, ze w typowych wodach naturalnych stężenia jonów wodorowych są bardzo niskie. Stężenie to zależy przede wszystkim od dysocjacji elektrolitycznej cząstek wody oraz od procesów dysocjacji i hydrolizy rozpuszczonych w niej związków. Chemicznie pH można zinterpretować jako zdolność roztworu do transferu protonów.
Podział wód podziemnych ze względu na ich odczyn przedstawia się następująco (wg Z. Pazdro i B Kozerskiego, 1990)
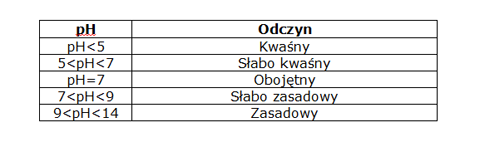
UTLENIALNOŚĆ KMnO4 – Pośrednią metoda oznaczenia zawartości ogólnego bądź rozpuszczonego węgla organicznego w wodzie jest określenie jaka ilość tlenu jest potrzebna do utlenienia substancji organicznych. Ta niezbędna ilość tlenu określana jest jako chemiczne zapotrzebowanie tlenu CHZT. Tlen dodawany jest do wody w formie silnego utleniacza a ilość zużytego tlenu podawana jest w mg O2/dm3. Utleniaczami są zazwyczaj nadmanganian potasu KMnO4 lub dwuchromian potasu K2Cr2O7. Utlenialność jest wskaźnikiem zanieczyszczenia wód substancjami organicznymi.
PEW – PRZEWODNOŚĆ ELEKTROLITYCZNA WŁAŚCIWA – określana potocznie przewodnością wody jest parametrem pozwalającym w przybliżeniu określić ilość rozpuszczonych substancji w wodzie. Praktycznie każda zmiana ilości substancji rozpuszczonych w wodzie wywołuje zmianę PEW. Jest to zatem bardzo przydatny wskaźnik pozwalający zarejestrować zmiany składu chemicznego wód, szczególnie wywołane zanieczyszczeniami. PEW bardzo ściśle zależy od temperatury. Zbadano, że przy wzroście temperatury wody o 10C następuje wzrost przewodności o 1,8 – 2,5% (A. Macioszczyk, D. Dobrzyński, 2007).
Aby móc interpretować pomiary PEW z różnych punktów poboru i z różnego okresu czasu przyjęto temperaturę 250C jako temperaturę odniesienia. Przewodność elektrolityczna właściwa wyrażana jest w S/m lub jednostkach pochodnych. Przewodność wyrażona w µS/cm jest tego samego rzędu wielkości co wartość mineralizacji wody w mg/l.
TWARDOŚĆ – zależy od obecności w wodzie wapnia i magnezu oraz pozostałych mikroelementów. W praktyce pod pojęciem twardości ogólnej rozumiemy sumę wapnia i magnezu w wodzie. Obecność innych metali ziem alkalicznych w stosunku do Ca i Mg jest tak mała, ze mieści się w granicach błędu oznaczeń. Ta część jonów wapnia i magnezu, które mogą występować jako kwaśne wodorowęglany (HCO3-) lub węglany (CO32-) określana jest mianem twardości węglanowej. Natomiast ta część jonów wapnia i magnezu która związana jest z siarczanami, chlorkami i azotanami itp. określana jest jako twardość niewęglanowa.
Twardość ogólna = Twardość węglanowa + Twardość niewęglanowa
Niekiedy w literaturze można spotkać pojęcie twardości przemijającej odpowiadającej w przybliżeniu twardości węglanowej oraz pojęcie twardości stałej (trwałej) odpowiadającej zakresem twardości nie węglanowej.
Twardość węglanowa zanika w wyniku gotowania wody. Natomiast twardość niewęglanową można usunąć z wody jedynie przy pomocy specjalnych metod chemicznych lub destylacji.
Zgodnie z obowiązującymi w Polsce przepisami sanitarnymi, jednostką wyrażania twardości wody jest mgCaCO3/dm3 wody. Obok tej jednostki często spotyka się podawanie twardości w miligramorównoważnikach jonów nadających twardość wodzie mval/dm3 lub w stopniach niemieckich (0n)
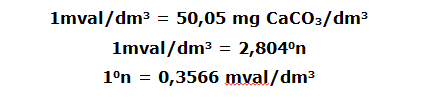
Podział wód podziemnych ze względu na twardość ogólną przedstawia się następująco
(A. Macioszczyk, D. Dobrzyński, 2007)
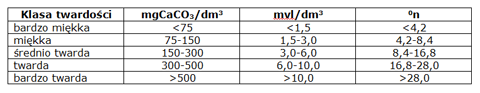
Twardość wody ma duże znaczenie z praktycznego i gospodarczego punktu widzenia. Wody zbyt twarde nie nadają się do zasilania kotłów parowych, instalacji centralnego ogrzewania. Wytrącający się kamień kotłowy niszczy urządzenia ciepłownicze i grzewcze, zmniejsza światło przewodów i powodują znaczne straty ciepła. Zbyt twarda woda powoduje zwiększone ilości zużycia mydła oraz detergentów oraz wpływa na smak i aromat przygotowywanych potraw (kawa, herbata) oraz znacznie wydłuża czas gotowania. Z kolei wody zbyt miękkie pływają znacząco na rozwój procesów korozyjnych w przewodach wodociągowych.
DWUTLENEK WĘGLA – to gaz bezbarwny o bardzo słabym zapachu około 1,5 razy cięższy od powietrza. Wykazuje stosunkowo dużą rozpuszczalność w wodzie i wchodzi z nią w reakcję, natomiast jego rozpuszczalność w wodzie spada wraz ze wzrostem temperatury. Dwutlenek węgla zwiększa zdolność rozpuszczania wielu minerałów przez wodę oraz sam jest źródłem powstawania jonów HCO3- i CO32-. Aby w roztworze utrzymała się ilość kwaśnych węglanów w formie rozpuszczonej potrzebna jest pewna ilość CO2 określana jako tzw. dwutlenek węgla równowagi. Cały nadmiar CO2 będzie powodował rozpuszczanie węglanu wapniowego i nosi nawę dwutlenku węgla agresywnego. Agresywność polega na właściwościach korozyjnych w stosunku do skał, minerałów węglanowych, betonu, żelaza i innych metali.
AZOT AMONOWY (NNH4) – Jon amonowy NH4+ oznacza w istocie sumę jonów NH4+ oraz amoniaku rozpuszczonego w wodzie NH3. Proporcje między tymi składnikami zależą od pH roztworu, temperatury oraz siły jonowej. Głównym źródłem jonów amonowych (azotu amonowego) w wodzie jest rozkład materii organicznej zawierającej azot (białka, mocznik, itp.) Pochodzenie materii może być ze źródeł naturalnych lub antropogenicznych zawierających substancje organiczne (nawozy organiczne, obornik, gnojowica, soki kiszonkowe, ścieki bytowe, odpady przemysłowe itp.) W głębszych wodach podziemnych azot amonowy może pochodzić oprócz rozkładu materii organicznej także z procesu denitryfikacji azotanów zawartych w wodach.
AZOTANY – anion NO3- jest jedną z najbardziej podstawowych form migracji azotu w wodach podziemnych. Azot należy do składników biogennych i ulega wielu przemianom w procesach tworzenia i rozkładu materii organicznej. Azotany mogą pochodzić z opadów atmosferycznych, rozkładu i mineralizacji substancji organicznych oraz substancji wprowadzanych w wyniku działalności człowieka (rolnictwo, gospodarka komunalna). Nadmiar azotanów w wodach pitnych stwarza poważne zagrożenie dla zdrowia ludzi szczególnie małych dzieci i niemowląt. Ponadnormatywne stężenia azotanów mogą wywoływać u niemowląt sinicę (methemoglobinemia). Układ pokarmowy niemowląt zawiera bakterie posiadające zdolność redukcji azotanów do trujących azotynów NO2-, które przechodząc do krwiobiegu tworzą z hemoglobiną methemoglobinę, która nie posiada zdolności przenoszenia tlenu. Może to wywołać niedotlenienie a nawet śmierć. U osób dorosłych nadmiar azotanów może przyczyniać się do rozwoju raka żołądka.
AZOTYNY – stanowią przejściową formę przemian jakim podlegają związki azotowe w wodach podziemnych. Głównym źródłem azotynów jest najczęściej rozkład organicznych związków azotowych naturalnych bądź antropogenicznych. Azotyny powstają w wyniku utleniania jonu amonowego NH4+ lub w wyniku redukcji azotanów NO3-. Obecność toksycznych azotynów świadczy, że procesy biochemicznego utleniania związków azotowych nie zostały jeszcze zakończone. Ich nietrwały charakter sprawia, że są istotnym wskaźnikiem świeżego zanieczyszczenia wód substancjami organicznymi. Przeważnie azotyny występują w wodach podziemnych w niewielkich ilościach, są nietrwałe a ich stężenie ściśle zależy od kinetyki reakcji cyklu azotowego.
CHLORKI - to najpowszechniejsza forma występowania chloru w przyrodzie. Zawartość chlorków w wodach podziemnych rośnie znacząco wraz ze wzrostem ogólnej mineralizacji wody. Sole chlorkowe posiadają wysoką rozpuszczalność w wodzie, natomiast zdysocjowane jony chlorkowe łatwo migrują w wodach podziemnych, dlatego w badaniach hydrogeochemicznych uznawane są za tzw. jony wskaźnikowe. Chlorki są bardzo ważnym wskaźnikiem zanieczyszczenia słodkich wód podziemnych. Wynika to z obecności podwyższonych stężeń chlorków w większości ścieków komunalnych, nawozach naturalnych, gnojowicy, odciekach ze składowisk komunalnych oraz ściekach przemysłowych.
SIARCZANY – anion SO4- stanowi podstawową formę migracji siarki w wodach podziemnych. Głównym źródłem siarczanów w wodach podziemnych są procesy ługowania i wietrzenia skał oraz procesy biochemiczne zachodzące w warstwach wodonośnych. W zależności od warunków utleniająco-redukcyjnych siarka może występować na 6 różnych stopniach utlenienia od H2S, S2-, do SO42-. Antropogeniczne źródła siarczanów związane są głównie z emisja SO2 do atmosfery, wpływem rolnictwa, niewłaściwą gospodarką wodno-ściekową, z odpadów komunalnych i przemysłowych.
ŻELAZO – może występować w wodzie w formie jonowej, kompleksowej, rozpuszczonej (dwu lub trój wartościowej), koloidalnej lub zawieszonej. Najpowszechniejsza formą występowania żelaza jest jon Fe2+. Wody natlenione są praktycznie pozbawione żelaza gdyż żelazo dwuwartościowe utlenia się i wytrąca w formie rdzawego osadu. Stężenie żelaza w wodach podziemnych jest zależne od pH oraz od Eh (potencjał utleniająco-redukcyjny). W środowisku redukcyjnym bardzo często pojawia się siarkowodór i wówczas żelazo może wytrącać się w postaci praktycznie nierozpuszczalnych siarczków. Żelazo nie jest składnikiem toksycznym. Jest dobrze przyswajalne przez organizm człowieka a jego nadmiar w wodzie powoduje głównie problemy natury organoleptycznej i estetycznej.
MANGAN – w wodach może występować na trzech stopniach utlenienia jako dwu, trój lub cztero-wartościowy. Jego stężenie zależy ściśle od pH oraz Eh (warunki utleniająco-redukcyjne). W typowych warunkach dominuje forma Mn2+ natomiast formy Mn3+ są nietrwałe a z kolei związki Mn4+ praktycznie nierozpuszczalna w wodzie. Zawartość manganu w wodach podziemnych jest zazwyczaj ograniczona rozpuszczalnością węglanów manganu. Mangan w wodzie jest bardziej stabilny niż żelazo. Mangan nie jest składnikiem toksycznym. Posiada bardzo duże znaczenie dietetyczne dla człowieka. Jest dobrze przyswajalny przez organizm człowieka a jego nadmiar w wodzie powoduje głównie problemy natury organoleptycznej i estetycznej.
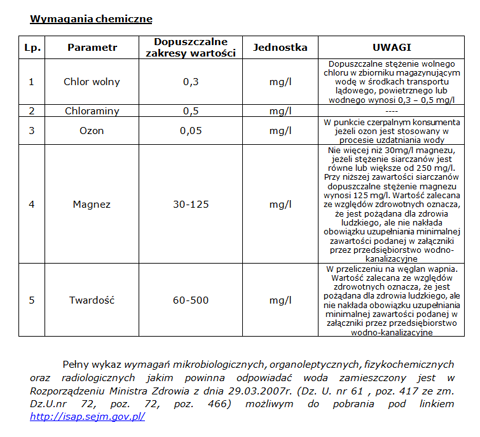
Przegląd wybranych wymagań mikrobiologicznych, organoleptycznych, fizykochemicznych oraz radiologicznych jakim powinna odpowiadać woda.
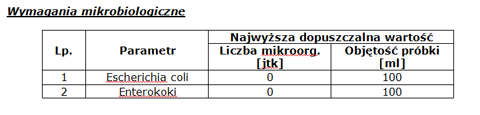
Od dnia 01 stycznia 2008r., należy badać ciepłą wodę użytkową w budynkach zbiorowego zamieszkania oraz zakładach opieki zdrowotnej zamkniętej na obecność bakterii z rodzaju Legionella. Występowaniu i namnażaniu się tych bakterii w instalacjach wodnych sprzyjają różne czynniki. Temperatura zbliżona do 400C, brak recyrkulacji, obecność osadów, biofilmu, stwarzają warunki sprzyjające rozwojowi pałeczek Legionella. Główne miejsca występowania tych mikroorganizmów to głównie zbiorniki akumulacyjne ciepłej wody, osady w separatorach i odmulaczach, ślepe odcinki sieci, a także elementy instalacji pokryte osadem wapiennym, kamieniem kotłowym takie jak prysznice, wylewki baterii, nasadki sitkowe baterii umywalkowych. Zachorowania wywołane przez pałeczki Legionella określane są jako legionellozy, a najczęściej występujące typy zachorowań to tzw. choroba legionistów (ciężkie zapalenie płuc) oraz gorączka Pontiac występująca w postaci epidemii. Objawy zachorowań to suchy duszący suchy kaszel, zaburzenia w oddychaniu, bardzo wysoka temperatura oraz zaburzenia świadomości.
Do przeprowadzenia dezynfekcji cieplnej i eliminacji bakterii chorobotwórczych z tej grupy niezbędne jest zapewnienie uzyskania w punktach czerpalnych temperatury wody nie niższej niż 70 °C i nie wyższej niż 80 °C." Bakterie Legionella w temperaturach wyższych niż +60 °C nie tylko się nie namnażają, ale bardzo szybko giną.
Zgodnie z § 120 ust. 2 Rozporządzenia Ministra Infrastruktury z dnia 12.04.2002r., w sprawie warunków technicznych, jakim powinny odpowiadać budynki i ich usytuowanie (Dz. U. z 2002 r., Nr 75, poz. 690 z poźn. Zm. - Dz. U. 2009 r., Nr 56, poz.461) instalacja ciepłej wody powinna zapewniać uzyskanie w punktach czerpalnych temperatury wody nie niższej niż 55°C i nie wyższej niż 60°C, przy czym instalacja ta powinna umożliwiać przeprowadzenie jej okresowej dezynfekcji termicznej przy temperaturze wody nie niższej niż 70°C

W zakładach opieki zdrowotnej zamkniętej na oddziałach, w których przebywają pacjenci o obniżonej odporności, w tym objęci leczeniem immunosupresyjnym, pałeczki Legionella sp. powinny być nieobecne w próbce wody o objętości 1000ml.